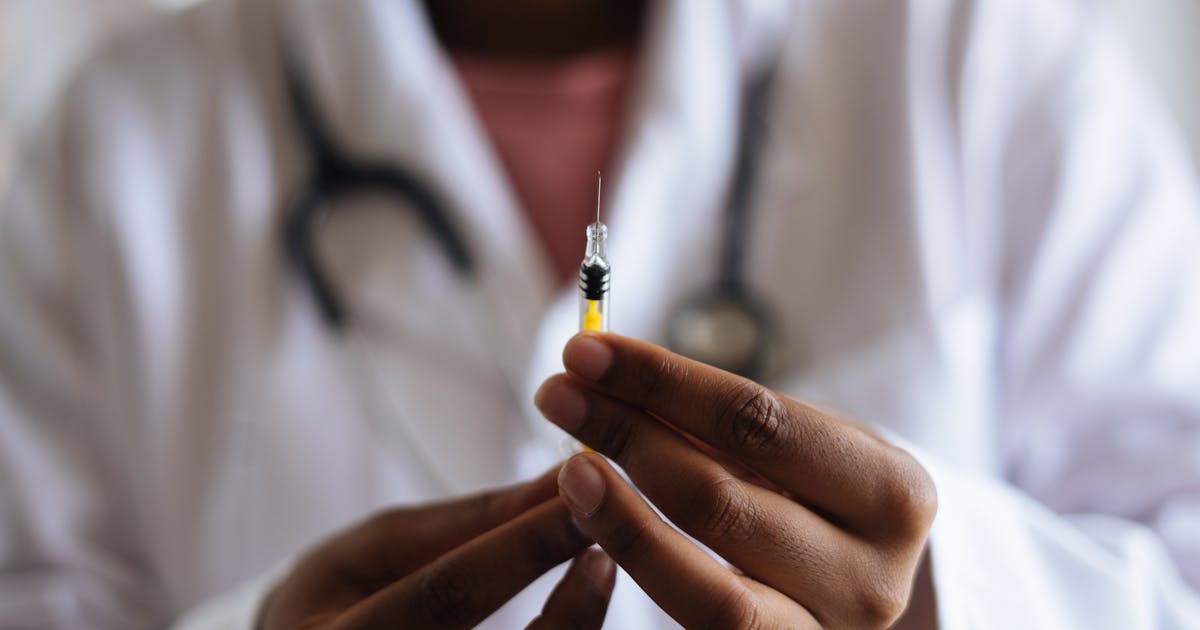
あなたをがんから守るワクチンが、あなただけのために作られるとしたら?長い間、SF小説の世界の話とされてきたこのシナリオが、2026年に現実となりつつあります。新型コロナウイルスとの戦いで有名になったメッセンジャーRNA(mRNA)ワクチンが、今日では腫瘍に対する精密な武器として生まれ変わっています。最初の臨床結果は目を見張るものがあり、科学界ではすでに最も悪性度の高いがんの治療における革命として語られています。
新型コロナからがんへ:mRNAが標的を変えた経緯
mRNA技術は2020年に一躍脚光を浴びました。BioNTechとModernaが記録的な速さでSARS-CoV-2ワクチンを開発したことがきっかけです。しかしその偉業の陰には、はるかに古いプロジェクトが潜んでいました。mRNAを使って免疫系ががん細胞を認識し破壊するよう訓練するという構想です。
その原理はエレガントです。各腫瘍は分子の指紋のような固有の遺伝子変異を持っています。個別化mRNAワクチンはこの特異性を活用します。患者の腫瘍生検から研究者が特定の変異を識別し、これらの標的をコードした個別ワクチンを製造します。接種されると、ワクチンは患者の細胞に腫瘍タンパク質の断片を産生するよう指令し、標的を絞った強力な免疫反応を引き起こします。
ゲームを変える臨床結果
2026年、いくつかのフェーズII臨床試験が注目すべき結果を示しています。ModernaのmRNA-4157(V940)プログラムは、ペムブロリズマブ(免疫療法薬)と組み合わせて、進行期メラノーマ患者における再発リスクの有意な低下を示しました。規制当局への申請書類は今年中に提出される見通しで、承認を受けた最初の治療的がんワクチンとなる可能性があります。
BioNTech側の結果も同様に心強いものです。彼らの候補BNT122は、最も攻撃的な乳がんの一形態であるトリプルネガティブ乳がん患者で試験され、ワクチン接種後数年間持続する強力で耐久性のある免疫反応を生み出しました。腫瘍特異的T細胞は治療後も長期間活性を維持しており、再発に対する長期的な防御効果が示唆されています。
膵臓がんの試験も進行中です。これは治療が最も困難ながんの一つで、5年生存率が10%未満です。ニューヨークのメモリアル・スローン・ケタリングがんセンターは、個別化mRNAワクチンが患者グループで持続的な免疫活性を誘導したと報告しており、これまで治療の選択肢が非常に限られていた分野に希望をもたらしています。
精度に奉仕する人工知能
2026年にこの進歩を可能にしているのは、分子生物学と人工知能の融合です。AIアルゴリズムは今や数時間で腫瘍ゲノムを解析し、効果的な免疫反応を引き起こす可能性が最も高い変異を特定します。ネオアンティジェン探索と呼ばれるこのステップは、かつては長く不確実なプロセスでした。今日、AIは生検後6週間以内に個別化ワクチンを設計することを可能にしています。
デリバリーシステムも進歩しました。次世代の脂質ナノ粒子はmRNAをよりよく保護し、免疫細胞へより正確に誘導することで、副作用を減らしながら有効性を高めています。CRISPRを統合したプラットフォームは、患者のT細胞の特定の遺伝子を編集することで免疫反応を最適化することすら可能にしています。
臨床開発中の候補が60種以上
世界のmRNAがんワクチンパイプラインは今や60種以上の臨床開発中の候補を超えています。Moderna、BioNTech、CureVac、そしてGritstone bioやNuvation Bioなどの新興企業がこの分野に多大な投資を行っています。標的は多岐にわたります。メラノーマ、大腸がん、非小細胞肺がん、神経膠芽腫、膵臓がん、乳がんなど。
最初の商業承認は2029年までに見込まれていますが、最も進んだプログラムは2027年には早くも加速承認を得られる可能性があります。リスクは莫大です。化学療法などの標準的治療とは異なり、個別化mRNAワクチンは悪性細胞のみを攻撃し、健康な組織を温存し、治療毒性を大幅に低減します。
まだ克服すべき課題
熱意が高まる一方で、重大な障害が依然として存在します。個別化ワクチンの製造コストは依然として高く、各投与量は単一の患者のために製造された独自の製品です。AIによって短縮されても生産期間は、週単位で状況が変わる急速進行性がんにとって問題です。
研究資金の問題も重要です。サイエンティフィック・アメリカンの最近の記事が指摘するように、米国連邦機関の予算削減は臨床試験を遅らせると懸念されています。これはかつてないほど有望な結果が出ている時期にもかかわらずです。欧州では、公的・民間資金は今のところより安定しており、製薬業界と大学病院センターとの積極的な協力関係が続いています。
最後に、患者間の免疫反応の変動性が依然として課題です。すべての生体がワクチンに同じ方法で反応するわけではなく、研究者は治療から最も恩恵を受ける患者をより適切に選択するための予測的バイオマーカーの特定に取り組んでいます。
がんとの戦いにおける新時代へ
個別化mRNAワクチンは単なる技術的進歩以上のものを表しています。それは医学におけるパラダイムシフトを体現しています。初めて、治療はがんの種類ではなく、各患者の固有の分子プロファイルによって決定されます。しばしば精密腫瘍学と呼ばれるこのアプローチは、がんをしばしば致命的な疾患から長期的に管理される慢性疾患へと変革する可能性があります。
最初の治療ワクチンが市場に近づく中、私たち一人一人に問いが生じます。真に個別化された医療の時代に入る準備ができているでしょうか?2026年の進展は、答えがイエスであることを示唆しています。そして、最良の時代はまだ来ていません。
 English
English  French
French  Spanish
Spanish  Chinese
Chinese  Japanese
Japanese  Korean
Korean  Hindi
Hindi  German
German  Norwegian
Norwegian