2025년 2월, KJ라는 이름의 영아가 의학의 역사를 바꿨습니다. 희귀하고 잠재적으로 치명적인 유전 질환을 앓고 있던 그는 완전히 개인화된 CRISPR 유전자 치료를 받은 사상 첫 번째 인간이 되었습니다. 1년 후, 그 결과는 모든 기대를 뛰어넘어 전 세계 수백만 환자들에게 혁명적인 길을 열어주었습니다.
치명적인 결과를 초래하는 희귀 질환
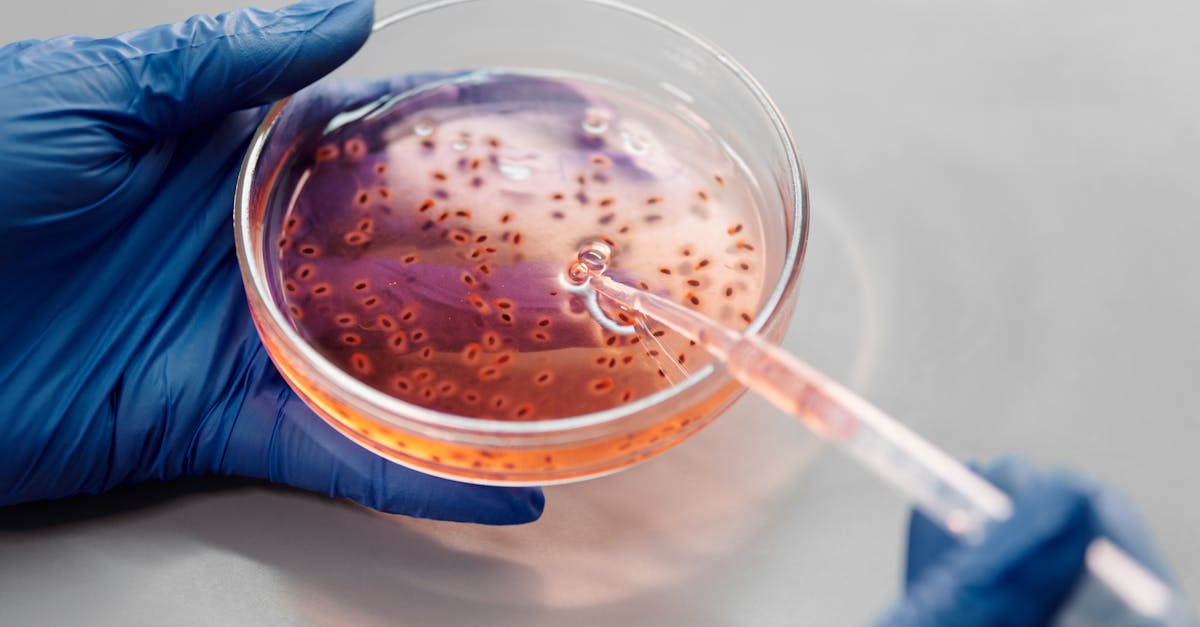
KJ는 카르바모일인산 합성효소 1(CPS1) 결핍증을 가지고 태어났습니다. 이는 약 130만 명 출생 중 1명꼴로 발생하는 유전성 대사 질환입니다. 간의 요소 회로에 필수적인 이 효소는 단백질 분해로 생성되는 암모니아를 제거하는 역할을 합니다. 이 효소가 없으면 암모니아가 혈액에 축적되어 비가역적인 뇌 손상이나 사망을 초래할 수 있습니다.
태어난 순간부터 KJ는 극도로 저단백 식이요법을 따르고, 견딜 수 있는 암모니아 수치를 유지하기 위해 강력한 질소 제거 약물을 복용해야 했습니다. 생후 불과 5개월에 그의 상태는 너무나 위태로워 간 이식 대기 명단에 올랐습니다. 이는 위험하고 부담이 큰 대형 수술이었으며, 이렇게 어린 환자에게 공여자 확보 가능성도 불확실했습니다.
맞춤 치료제를 만드는 데 걸린 6개월
필라델피아 아동병원(CHOP)의 Rebecca Ahrens-Nicklas 박사 팀은 전례 없는 도전에 나섰습니다. 단 6개월 만에 개인화된 유전자 편집 치료를 설계, 제조, 투여하는 것이었습니다. 사용된 기술은 염기 편집이라 불리며, 고전적 CRISPR의 발전형입니다. 분자 가위처럼 DNA를 절단하는 대신, 염기 편집은 이중 가닥 절단을 일으키지 않고 외과적 정밀도로 유전 암호의 단 한 글자를 수정합니다.
치료제는 지질 나노입자에 캡슐화되었습니다. mRNA 백신에 사용된 것과 동일한 기술로, KJ의 간세포에 직접 전달하기 위해서입니다. 목표는 CPS1 효소 기능 장애를 유발하는 돌연변이를 교정하고, 암모니아를 제거하는 능력을 부분적으로 회복시키는 것이었습니다.
1년 후의 고무적인 결과
2025년 2월 25일, KJ는 첫 번째 주입을 받았습니다. 3월과 4월에 두 번의 추가 투여가 이어졌습니다. Ahrens-Nicklas 박사는 다음과 같이 말했습니다. "이 치료법이 최종 완치는 아니지만, 세 번의 주입 후 KJ는 심각한 부작용 없이 잘 견뎌냈습니다."
1년 후, 진전은 놀랍습니다. KJ는 걷고, 말하며, 또래에 맞는 발달 이정표를 달성하고 있습니다. 식단에 단백질을 늘릴 수 있게 되었고, 질소 제거 약물의 용량도 줄었습니다. 소아 질환 에피소드 중에도——암모니아가 급등할 수 있는 위급한 순간에도——그의 수치는 통제 범위 내에 유지되었습니다.
접근을 가속화하는 규제 혁명
KJ의 이야기는 의학 연구만 변화시키는 것이 아니라 규제에도 영향을 미칩니다. 2026년 2월 23일, 미국 FDA는 "그럴듯한 메커니즘"이라는 새로운 승인 체계를 발표했습니다. 이 제도는 기존 임상시험에서 통상 요구되는 수백 명이 아닌, 불과 5~10명의 환자만으로도 개인화 치료를 승인할 수 있도록 합니다. 전통적인 시험을 위해 충분한 환자를 모으는 것이 때로는 불가능한 초희귀 질환에 있어 결정적인 진전입니다.
CHOP 팀은 2026년에 여러 요소 회로 장애를 아우르는 확장 플랫폼에 대한 1/2상 임상시험 신청서를 제출할 계획입니다. GTIMD(유전성 대사 질환 유전자 치료) 프로그램은 이미 유기산혈증, 지방산 산화 결함, 페닐케톤뇨증에 대한 응용을 연구 중입니다.
내일의 의학을 위한 모델
KJ의 사례가 진정으로 혁명적인 이유는 치료 자체뿐만 아니라 그것이 열어젖히는 모델에 있습니다. 지금까지 약물 개발에는 평균 10~15년이 걸리고 수십억 달러의 비용이 들었습니다. 여기서는 단 6개월 만에 한 명의 환자를 위한 맞춤 치료가 만들어졌습니다. 이 과정이 산업화되고 접근 가능해진다면, 희귀 질환 의학 전반이 변혁될 수 있습니다.
KJ를 치료한 팀의 핵심 과학자는 2026년 1월 Aurora Therapeutics라는 스타트업을 창립하여 개인화 CRISPR 치료 생산의 대중화를 목표로 삼았습니다. 목표는 비용과 일정을 줄여서 희귀 유전 질환을 가진 모든 환자가 언젠가 자신의 돌연변이에 특화된 치료를 받을 수 있도록 하는 것입니다.
가족의 희망과 행동 촉구
KJ의 부모 Kyle과 Nicole Muldoon은 유전자 치료 연구의 옹호자가 되었습니다. Nicole은 이렇게 밝혔습니다. "입법자들은 연구에 투자하고 의료 접근성을 확대함으로써 이것을 가능하게 할 수 있습니다." 그들의 증언은 과학적 진보 뒤에 매일매일이 소중한 가족들이 있다는 것을 상기시켜 줍니다.
전 세계적으로 7,000개 이상의 유전성 희귀 질환이 3억~4억 명에게 영향을 미치는 것으로 추정됩니다. 그 대다수에게는 특정 치료법이 존재하지 않습니다. KJ로부터 시작된 이 접근법은 궁극적으로 이 환자 한 사람 한 사람에게 희망의 빛을 제공할 수 있습니다.
아기 KJ의 이야기는 단순한 의학적 위업이 아닙니다. 그것은 의학이 새로운 시대로 접어드는 신호입니다. 치료가 환자를 위해 설계되는 시대, 그 반대가 아닌. 우리 DNA라는 위대한 책 속에서, 한 글자 한 글자 조용히 진행되는 혁명입니다.
 Korean
Korean  French
French  English
English  Spanish
Spanish  Chinese
Chinese  Japanese
Japanese  Hindi
Hindi  German
German  Norwegian
Norwegian