2025年2月,一名名叫KJ的婴儿改写了医学史。他患有一种罕见且可能致命的遗传病,成为有史以来第一个接受完全个性化CRISPR基因治疗的人。一年后,治疗结果超出所有人的预期,为全球数百万患者开辟了一条革命性的道路。
一种后果严重的罕见病
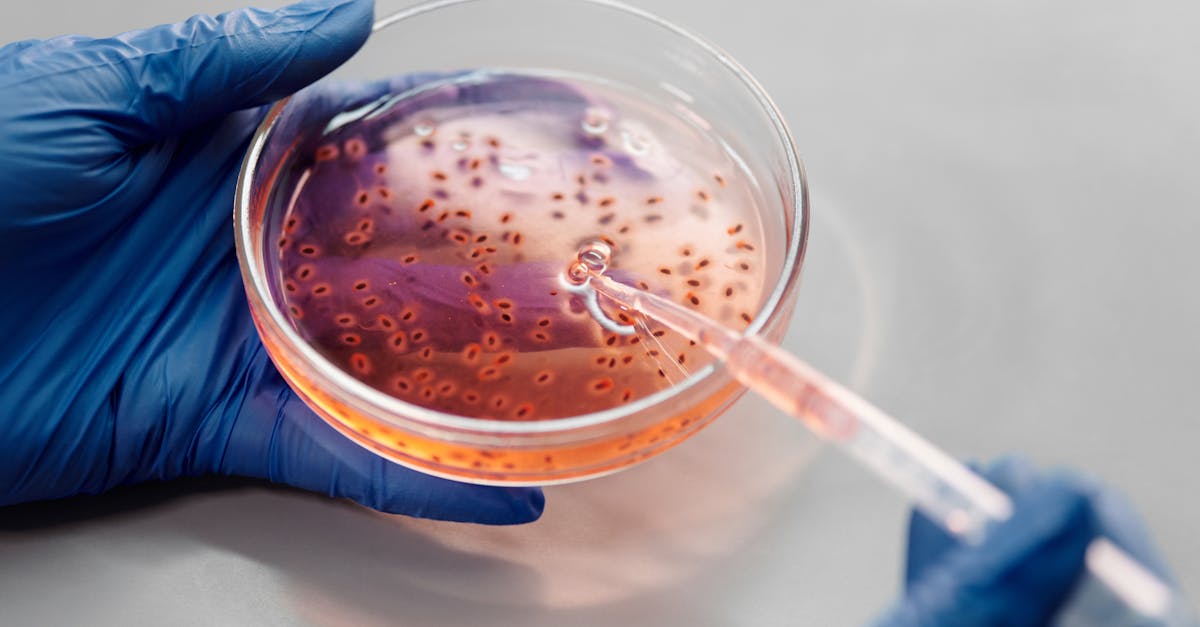
KJ出生时患有氨甲酰磷酸合成酶1(CPS1)缺乏症,这是一种遗传性代谢疾病,发病率约为每130万新生儿中1例。这种酶对肝脏中的尿素循环至关重要,通常负责清除蛋白质代谢产生的氨。没有这种酶,氨就会在血液中积聚,可能导致不可逆的脑损伤甚至死亡。
KJ自出生起就必须严格遵循极低蛋白质饮食,并服用强效的氮清除药物以维持可耐受的氨水平。年仅五个月时,他的病情已经岌岌可危,被列入肝脏移植等待名单——这是一项风险极高的大型手术,而且对如此年幼的患者来说,供体的可获得性也充满不确定性。
六个月打造定制化治疗方案
费城儿童医院(CHOP)的Rebecca Ahrens-Nicklas博士团队接受了一项前所未有的挑战:在短短六个月内设计、制造并实施一种个性化基因编辑疗法。所采用的技术称为碱基编辑,是经典CRISPR的升级版。与像分子剪刀一样切割DNA不同,碱基编辑以外科手术般的精确度修改遗传密码中的单个碱基字母,而不会造成双链断裂。
该治疗被封装在脂质纳米颗粒中——与mRNA疫苗所用的技术相同——以便直接递送到KJ的肝细胞。目标是:纠正导致CPS1酶功能障碍的突变,部分恢复其清除氨的能力。
一年后令人鼓舞的结果
2025年2月25日,KJ接受了第一次输注。3月和4月又相继接受了两次追加剂量。Ahrens-Nicklas博士指出:"虽然这种治疗不是最终治愈方法,但在三次输注后,KJ耐受良好,没有出现严重的副作用。"
一年后,进展显著。KJ能够行走、说话,达到了同龄儿童应有的发育里程碑。他的饮食中蛋白质含量得以增加,氮清除药物的剂量也有所减少。即使在儿童疾病发作期间——氨水平可能急剧上升的关键时刻——他的指标也保持在可控范围内。
加速获取渠道的监管革命
KJ的故事不仅改变了医学研究,也影响着监管政策。2026年2月23日,美国FDA宣布了一项名为"合理机制"的新审批框架。该机制允许仅凭5至10名患者的数据就授权个性化疗法,而非传统临床试验通常要求的数百名患者。对于超罕见疾病来说,这是决定性的进步——因为有时根本不可能为传统试验招募到足够多的患者。
CHOP团队计划在2026年提交一项I/II期临床试验申请,涵盖多种尿素循环障碍的扩展平台。GTIMD(遗传代谢疾病基因治疗)项目已在探索有机酸血症、脂肪酸氧化缺陷和苯丙酮尿症的应用。
未来医学的范本
KJ案例之所以真正具有革命性,不仅在于治疗本身,更在于它所开创的模式。以往,一种药物的研发平均需要十到十五年,耗资数十亿美元。而在这里,一种定制化治疗在六个月内为单个患者量身打造。如果这一过程能够产业化并实现可及性,整个罕见病医疗领域都将被彻底改变。
治疗KJ团队中的一位核心科学家于2026年1月创立了Aurora Therapeutics公司,致力于普及个性化CRISPR疗法的生产。目标是:降低成本和缩短时间线,让每一位罕见遗传病患者有朝一日都能受益于专门针对其突变设计的治疗方案。
家庭的希望与行动的召唤
KJ的父母Kyle和Nicole Muldoon已成为基因治疗研究的倡导者。Nicole表示:"立法者可以通过投资研究、扩大医疗获取渠道来实现这一目标。"他们的证词提醒我们,科学进步的背后,是无数将每一天都视为珍贵的家庭。
据估计,全球有超过7000种罕见遗传病,共影响3亿至4亿人。其中绝大多数至今没有特异性治疗方案。以KJ为起点开创的这一疗法,最终可能为每一位患者带来希望的曙光。
婴儿KJ的故事不仅仅是一项医学壮举,它是医学进入新时代的信号——在这个时代,治疗方案是为患者量身定制的,而非反过来。这是一场无声的革命,在我们DNA这本伟大的书中,一个碱基一个碱基地悄然进行。
 Chinese
Chinese  French
French  English
English  Spanish
Spanish  Japanese
Japanese  Korean
Korean  Hindi
Hindi  German
German  Norwegian
Norwegian