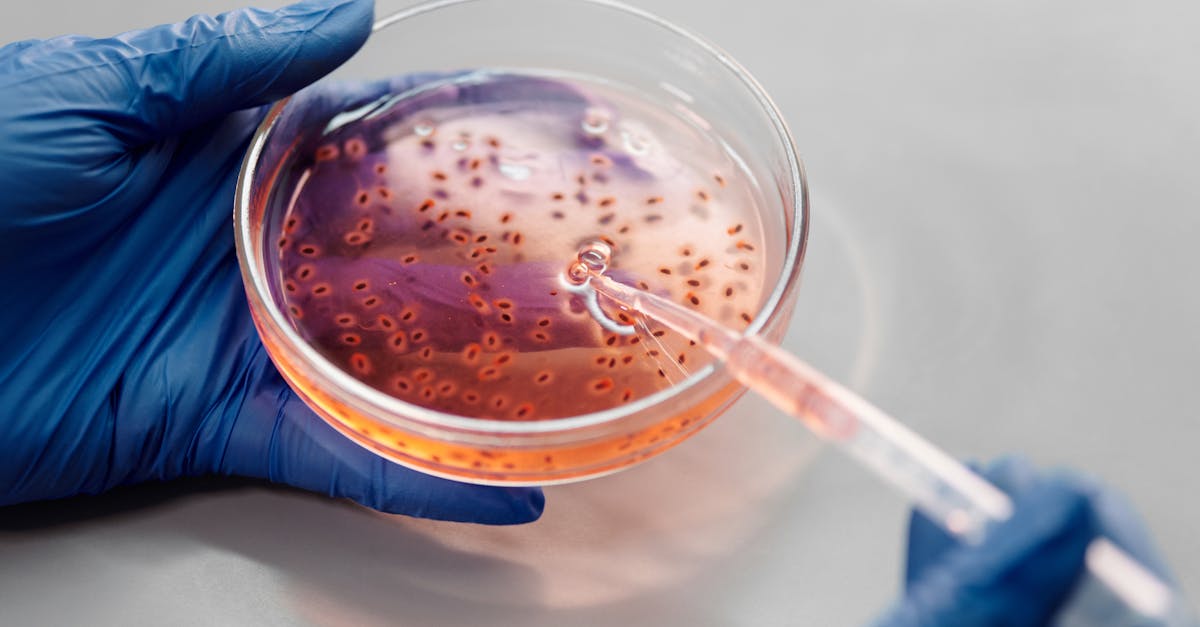
En febrero de 2025, un lactante llamado KJ entró en la historia de la medicina. Afectado por una enfermedad genética rara y potencialmente mortal, se convirtió en el primer ser humano en recibir una terapia génica CRISPR completamente personalizada. Un año después, los resultados superan todas las expectativas y abren un camino revolucionario para millones de pacientes en todo el mundo.
Una enfermedad rara con consecuencias devastadoras
KJ nació con un déficit de carbamoil fosfato sintetasa 1 (CPS1), una enfermedad metabólica hereditaria que afecta aproximadamente a 1 de cada 1,3 millones de nacimientos. Esta enzima, esencial para el ciclo de la urea en el hígado, normalmente elimina el amoniaco producido por la degradación de proteínas. Sin ella, el amoniaco se acumula en la sangre y puede provocar daños cerebrales irreversibles o incluso la muerte.
Desde su nacimiento, KJ tuvo que seguir una dieta extremadamente baja en proteínas y tomar potentes medicamentos eliminadores de nitrógeno para mantener niveles de amoniaco tolerables. Con tan solo cinco meses, su estado era tan precario que fue incluido en la lista de espera para un trasplante de hígado — un procedimiento quirúrgico mayor, arriesgado, y con disponibilidad incierta para un paciente tan pequeño.
Seis meses para crear un tratamiento a medida
Fue en el Children's Hospital of Philadelphia (CHOP) donde el equipo de la doctora Rebecca Ahrens-Nicklas asumió un desafío sin precedentes: diseñar, fabricar y administrar una terapia de edición genética personalizada en solo seis meses. La tecnología utilizada, llamada edición de bases, es una evolución del CRISPR clásico. En lugar de cortar el ADN como unas tijeras moleculares, la edición de bases modifica una sola letra del código genético con precisión quirúrgica, sin provocar una rotura de doble cadena.
El tratamiento fue encapsulado en nanopartículas lipídicas — la misma tecnología utilizada para las vacunas de ARNm — para entregarlo directamente a las células del hígado de KJ. El objetivo: corregir la mutación responsable del mal funcionamiento de la enzima CPS1 y restaurar parcialmente su capacidad para eliminar el amoniaco.
Resultados alentadores un año después
El 25 de febrero de 2025, KJ recibió su primera infusión. Dos dosis adicionales siguieron en marzo y abril. Como señaló la doctora Ahrens-Nicklas: "Aunque este tratamiento no es una cura definitiva, después de tres infusiones, KJ lo ha tolerado bien sin efectos secundarios graves."
Un año después, el progreso es notable. KJ camina, habla y alcanza los hitos de desarrollo esperados para su edad. Su dieta ha podido enriquecerse con proteínas, y las dosis de medicamentos eliminadores de nitrógeno han sido reducidas. Incluso durante episodios de enfermedad infantil — momentos críticos en que el amoniaco puede dispararse — sus niveles se mantuvieron bajo control.
Una revolución regulatoria para acelerar el acceso
La historia de KJ no solo transforma la investigación médica, sino que también influye en la regulación. El 23 de febrero de 2026, la FDA estadounidense anunció un nuevo marco de aprobación denominado "mecanismo plausible". Este dispositivo permite autorizar terapias personalizadas con solo 5 a 10 pacientes, en lugar de los cientos habitualmente requeridos en los ensayos clínicos tradicionales. Un avance decisivo para las enfermedades ultra-raras, donde a veces es imposible reunir suficientes pacientes para un ensayo tradicional.
El equipo de CHOP planea presentar una solicitud de ensayo clínico de fase I/II en 2026 para una plataforma ampliada que cubra varios trastornos del ciclo de la urea. El programa GTIMD (Gene Therapy for Inherited Metabolic Disorders) ya estudia aplicaciones para las acidemias orgánicas, los defectos de oxidación de ácidos grasos y la fenilcetonuria.
Un modelo para la medicina del mañana
Lo que hace verdaderamente revolucionario el caso de KJ no es solo la terapia en sí, sino el modelo que inaugura. Hasta ahora, desarrollar un medicamento tomaba en promedio diez a quince años y costaba varios miles de millones. Aquí, un tratamiento a medida fue creado en seis meses para un solo paciente. Si este proceso puede industrializarse y hacerse accesible, es toda la medicina de las enfermedades raras la que podría transformarse.
Un científico clave del equipo que trató a KJ lanzó en enero de 2026 una startup, Aurora Therapeutics, con la ambición de democratizar la producción de terapias CRISPR personalizadas. El objetivo: reducir costos y plazos para que cada paciente con una enfermedad genética rara pueda algún día beneficiarse de un tratamiento diseñado específicamente para su mutación.
La esperanza de las familias y el llamado a la acción
Los padres de KJ, Kyle y Nicole Muldoon, se han convertido en portavoces de la investigación en terapia génica. Nicole declaró: "Los legisladores pueden hacer esto posible invirtiendo en investigación y ampliando el acceso a la atención." Su testimonio recuerda que detrás de los avances científicos, hay familias para quienes cada día cuenta.
Se estima que más de 7.000 enfermedades raras de origen genético afectan colectivamente a entre 300 y 400 millones de personas en todo el mundo. Para la gran mayoría de ellas, no existe ningún tratamiento específico. El enfoque inaugurado con KJ podría, a largo plazo, ofrecer un rayo de esperanza a cada uno de estos pacientes.
La historia del bebé KJ no es solo una proeza médica. Es la señal de que la medicina entra en una nueva era — aquella en la que el tratamiento se diseña para el paciente, y no al revés. Una revolución silenciosa, letra por letra, en el gran libro de nuestro ADN.
 Spanish
Spanish  French
French  English
English  Chinese
Chinese  Japanese
Japanese  Korean
Korean  Hindi
Hindi  German
German  Norwegian
Norwegian