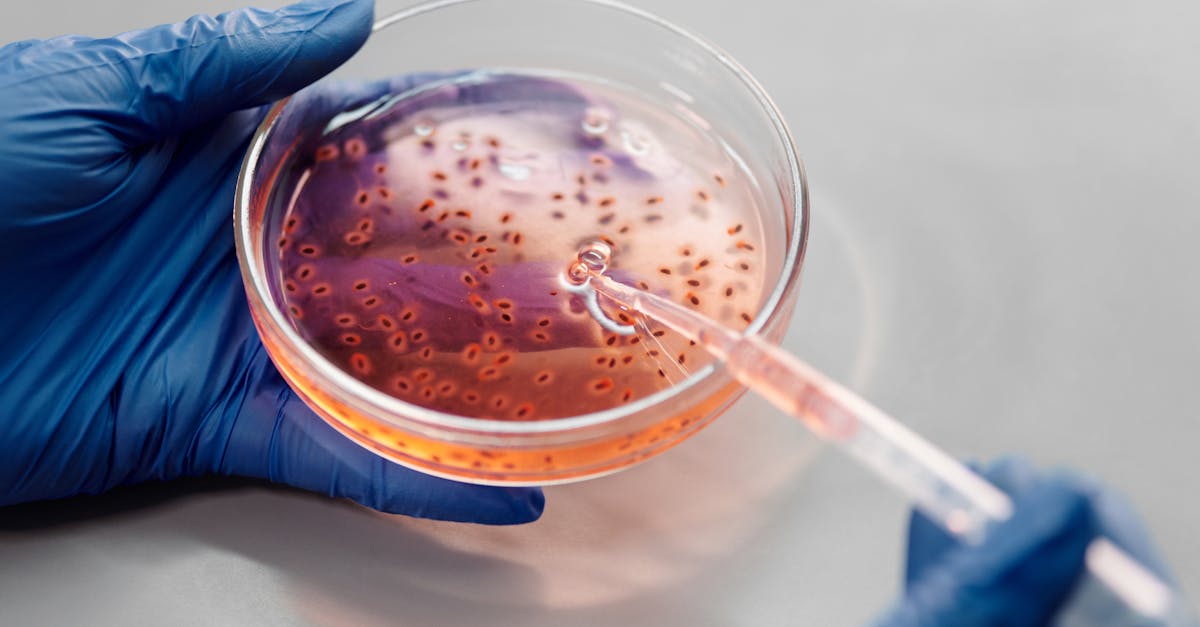
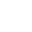I februar 2025 gikk en spedbarn ved navn KJ inn i medisinens historie. Han led av en sjelden og potensielt dødelig genetisk sykdom og ble det aller første mennesket til å motta en fullt personalisert CRISPR-genterapi. Ett år senere overgår resultatene alle forventninger og åpner en revolusjonerende vei for millioner av pasienter verden over.
En sjelden sykdom med ødeleggende konsekvenser
KJ ble født med mangel på karbamylfosfatsyntase 1 (CPS1), en arvelig stoffskiftesykdom som rammer omtrent 1 av 1,3 millioner fødsler. Dette enzymet, som er essensielt for ureasyklusen i leveren, fjerner normalt ammoniakken som produseres ved nedbrytning av proteiner. Uten det akkumuleres ammoniakk i blodet og kan forårsake irreversibel hjerneskade eller død.
Fra fødselen av måtte KJ følge et ekstremt proteinfattig kosthold og ta kraftige nitrogenscavengende medikamenter for å opprettholde tolerable ammoniakknivåer. I bare fem måneder gammel var tilstanden hans så prekær at han ble satt på ventelisten for levertransplantasjon — et stort kirurgisk inngrep, risikabelt, og med uforutsigbar tilgjengelighet for en så ung pasient.
Seks måneder for å skape en skreddersydd behandling
Det var ved Children's Hospital of Philadelphia (CHOP) at teamet til Dr. Rebecca Ahrens-Nicklas tok på seg en enestående utfordring: å designe, produsere og administrere en personalisert genredigeringsterapi på bare seks måneder. Teknologien som ble brukt, kalt basredigering, er en videreutvikling av klassisk CRISPR. I stedet for å kutte DNA som molekylære saks, modifiserer basredigering en enkelt bokstav i den genetiske koden med kirurgisk presisjon, uten å forårsake dobbelttrådbrudd.
Behandlingen ble innkapslet i lipidnanopartikler — den samme teknologien som brukes til mRNA-vaksiner — for å levere den direkte til KJs leverceller. Målet: å korrigere mutasjonen som er ansvarlig for CPS1-enzymets dysfunksjon og delvis gjenopprette dets evne til å eliminere ammoniakk.
Oppmuntrende resultater ett år senere
Den 25. februar 2025 fikk KJ sin første infusjon. To ytterligere doser fulgte i mars og april. Som Dr. Ahrens-Nicklas påpekte: "Selv om denne behandlingen ikke er en definitiv kur, har KJ etter tre infusjoner tolerert den godt uten alvorlige bivirkninger."
Ett år senere er fremgangen bemerkelsesverdig. KJ går, snakker og når de forventede utviklingsmilepælene for sin alder. Kostholdet hans har kunnet berikes med proteiner, og dosene av nitrogenscavengende medikamenter er blitt redusert. Selv under episoder med barnesykdom — kritiske øyeblikk der ammoniakk kan stige bratt — forble nivåene hans under kontroll.
En regulatorisk revolusjon for å fremskynde tilgangen
KJs historie transformerer ikke bare medisinsk forskning; den påvirker også reguleringen. Den 23. februar 2026 kunngjorde den amerikanske FDA et nytt godkjenningsrammeverk kalt "plausibel mekanisme". Denne mekanismen gjør det mulig å godkjenne personaliserte terapier basert på bare 5 til 10 pasienter, i stedet for de hundrevis som vanligvis kreves i tradisjonelle kliniske studier. Et avgjørende fremskritt for ultrasjelne sykdommer, der det noen ganger er umulig å samle nok pasienter til en tradisjonell studie.
CHOP-teamet planlegger å sende inn en søknad om fase I/II klinisk studie i 2026 for en utvidet plattform som dekker flere ureasyklus-forstyrrelser. GTIMD-programmet (Genterapi for arvelige stoffskiftesykdommer) utforsker allerede bruksområder for organiske asidemier, fettoksidasjonsdefekter og fenylketonuri.
En modell for morgendagens medisin
Det som gjør KJs tilfelle virkelig revolusjonerende, er ikke bare selve terapien, men modellen den innvarsler. Hittil tok det i gjennomsnitt ti til femten år å utvikle et legemiddel, og det kostet flere milliarder. Her ble en skreddersydd behandling laget på seks måneder for én enkelt pasient. Hvis denne prosessen kan industrialiseres og gjøres tilgjengelig, er det hele feltet for sjeldne sykdommer som kan bli transformert.
En nøkkelvitenskapsmann fra teamet som behandlet KJ, lanserte i januar 2026 en oppstart, Aurora Therapeutics, med ambisjonen om å demokratisere produksjonen av personaliserte CRISPR-terapier. Målet: å redusere kostnader og tidslinjer slik at hver pasient med en sjelden genetisk sykdom en dag kan dra nytte av en behandling designet spesifikt for sin mutasjon.
Familiers håp og oppfordring til handling
KJs foreldre, Kyle og Nicole Muldoon, har blitt talsmenn for generapiforskning. Nicole uttalte: "Lovgivere kan gjøre dette mulig ved å investere i forskning og utvide tilgangen til behandling." Deres vitnesbyrd minner oss om at bak vitenskapelige fremskritt er det familier for hvem hver dag teller.
Det anslås at mer enn 7 000 sjeldne genetiske sykdommer kollektivt rammer mellom 300 og 400 millioner mennesker verden over. For det store flertallet av dem finnes det ingen spesifikk behandling. Tilnærmingen som ble innvarslet med KJ, kunne til slutt gi et glimt av håp til hver enkelt av disse pasientene.
Baby KJs historie er ikke bare en medisinsk bragd. Det er signalet om at medisinen går inn i en ny æra — en der behandlingen er designet for pasienten, og ikke omvendt. En stille revolusjon, bokstav for bokstav, i vår DNAs store bok.
 Japanese
Japanese  French
French  English
English  Spanish
Spanish  Chinese
Chinese  Korean
Korean  Hindi
Hindi  German
German  Norwegian
Norwegian